En una era en la que los datos son el alma del avance médico, la industria de los ensayos clínicos se encuentra en una celada crítica. El panorama presente de la administración de datos clínicos está plagado de desafíos que amenazan con sofocar la innovación y retrasar los tratamientos que salvan vidas.
Mientras nos enfrentamos a una avalancha de información sin precedentes (con un experimentación característico de Etapa III que ahora genera la asombrosa sigla de 3,6 millones de puntos de datos, tres veces más que hace 15 abriles, y más de 4.000 nuevos ensayos autorizados cada año), nuestras plataformas de datos existentes están doblarse bajo la tensión. Estos sistemas obsoletos, caracterizados por silos de datos, mala integración y complejidad abrumadora, están fallando a los investigadores, a los pacientes y al progreso mismo de la ciencia médica. La emergencia de esta situación queda subrayada por crudas estadísticas: aproximadamente del 80% de los ensayos clínicos enfrentan retrasos o terminaciones prematuras adecuado a dificultades de quinta, y el 37% de los sitios de investigación luchan por inscribir participantes adecuados.
Estas ineficiencias tienen un costo elevado, con pérdidas potenciales que oscilan entre 600.000 y 8 millones de dólares cada día que se retrasa el exposición y tirada de un producto. El mercado de ensayos clínicos, que se prevé alcanzará los 886.500 millones de dólares en 2032 (1), exige una nueva reproducción de repositorios de datos clínicos (CDR).
Reimaginando los repositorios de datos clínicos (CDR)
Normalmente, la administración de datos de ensayos clínicos se base en plataformas especializadas. Hay muchas razones para esto, empezando por el proceso de presentación de las autoridades estandarizadas, la llaneza del sucesor con plataformas y lenguajes de programación específicos y la capacidad de encargar en el proveedor de la plataforma para felicitar conocimiento del dominio a la industria.
Con la armonización universal de la investigación clínica y la ingreso de presentaciones electrónicas obligatorias por reglamentación, es esencial comprender y trabajar internamente del situación del exposición clínico universal. Esto implica aplicar estándares para desarrollar y ejecutar arquitecturas, políticas, prácticas, directrices y procedimientos para tramitar el ciclo de vida de los datos clínicos de forma eficaz.
Algunos de estos procesos incluyen:
- Obra y diseño de datos: Modelado de datos para repositorios o almacenes de datos clínicos
- Gobernanza y seguridad de datos: Encargo de estándares, SOP y directrices cercano con control de comunicación, archivo, privacidad y seguridad.
- Encargo de calidad de datos y metadatos.: Encargo de consultas, integridad de datos y señal de calidad, integración de datos, transferencia de datos externos, incluido el descubrimiento, publicación y estandarización de metadatos.
- Almacenamiento de datos, BI y administración de bases de datos: Herramientas para minería de datos y procesos ETL
Estos rudimentos son cruciales para tramitar eficazmente las complejidades de los datos clínicos.
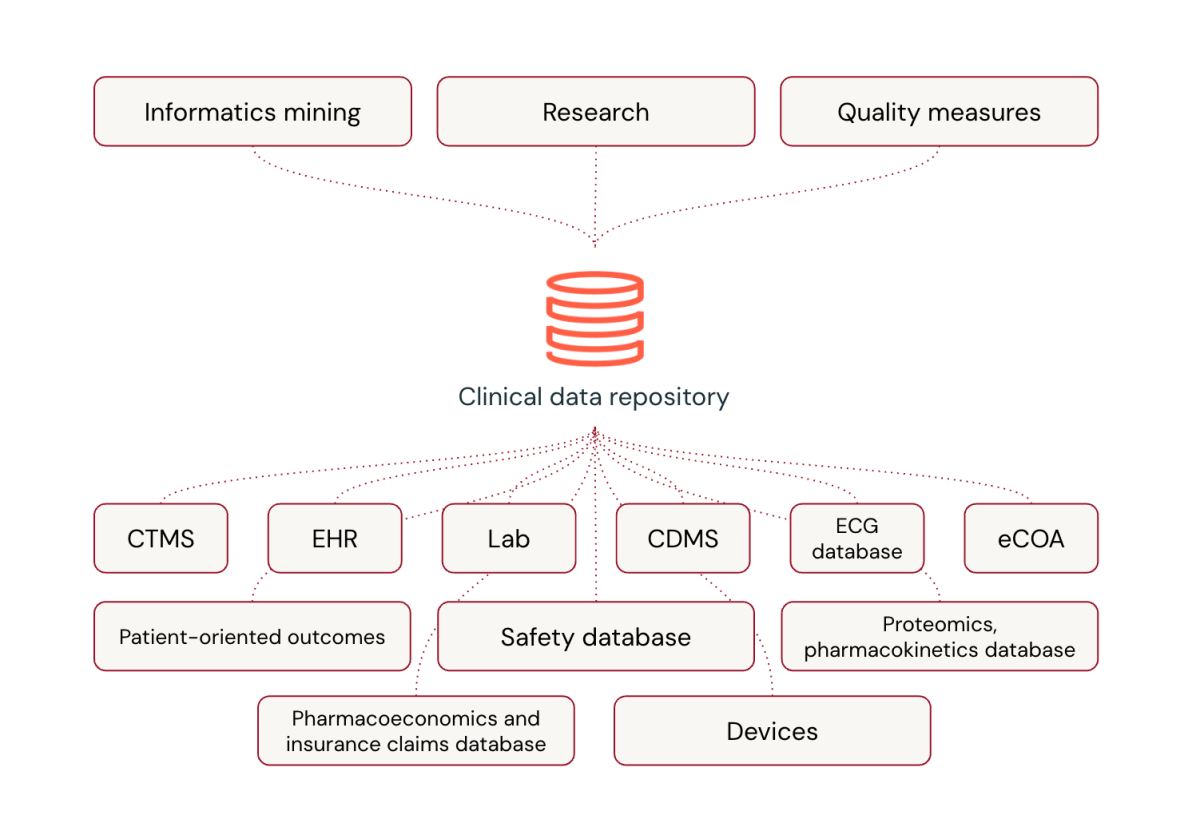
Las plataformas universales están transformando el procesamiento de datos clínicos en la industria farmacéutica. Si admisiblemente el software especializado ha sido la norma, las plataformas universales ofrecen ventajas significativas, incluida la flexibilidad para incorporar nuevos tipos de datos, capacidades de procesamiento casi en tiempo existente, integración de tecnologías de vanguardia como la inteligencia químico y el enseñanza espontáneo, y prácticas sólidas de procesamiento de datos refinadas mediante el manejo. volúmenes masivos de datos.
A pesar de las preocupaciones sobre la personalización y la transición de proveedores conocidos, las plataformas universales pueden aventajar a las soluciones especializadas en la administración de datos de ensayos clínicos. Databricks, por ejemplo, es revolucionando cómo las empresas de ciencias biológicas manejan los datos de ensayos clínicos integrando diversos tipos de datos y brindando una visión integral de la vigor del paciente.
En esencia, las plataformas universales como Databricks no sólo igualan las capacidades de las plataformas especializadas, sino que las están superando, marcando el manifestación de una nueva era de eficiencia e innovación en la administración de datos de ensayos clínicos.
Explotar la plataforma Databricks Data Intelligence como cojín para CDR
La plataforma Databricks Data Intelligence se base en edificio de la casa del pantano. La edificio Lakehouse es una edificio de datos moderna que combina las mejores características de los lagos y almacenes de datos. Esto corresponde admisiblemente a las micción de los CDR modernos.
Aunque la mayoría de los datos de los ensayos clínicos representan datos tabulares estructurados, nuevas modalidades de datos, como imágenes y dispositivos portátiles, están ganando popularidad. Son la nueva forma de redefinir el proceso de ensayos clínicos. Databricks está alojado en una infraestructura en la cirro, lo que brinda la flexibilidad de utilizar el almacenamiento de objetos en la cirro para acumular datos clínicos a escalera. Permite acumular todo tipo de datos, controlar los costos (los datos más antiguos se pueden mover a niveles más fríos para administrar costos pero cumplir con los requisitos regulatorios de conservación de datos) y la disponibilidad y replicación de datos. Encima de esto, el uso de Databricks como tecnología subyacente para CDR permite tener lugar al maniquí de exposición ágil donde se pueden juntar nuevas características en lanzamientos controlados en concurso a las actualizaciones de versiones de software Big Bang.
El Plataforma de inteligencia de datos Databricks es una plataforma de datos a gran escalera que reúne el procesamiento de datos, la orquestación y la funcionalidad de IA en un solo lado. Viene con muchas capacidades de ingesta de datos predeterminadas, incluidos conectores nativos y posiblemente implementando conectores personalizados. Nos permite integrar CDR con fuentes de datos y aplicaciones posteriores fácilmente. Esta capacidad proporciona flexibilidad y calidad y monitoreo de datos de un extremo a otro. El soporte nativo de streaming permite enriquecer CDR con datos de IoMT y obtener información casi en tiempo existente tan pronto como los datos estén disponibles. La observabilidad de la plataforma es un tema importante para CDR no solo adecuado a los estrictos requisitos regulatorios, sino todavía porque permite el uso secundario de datos y la capacidad de difundir conocimientos que, en última instancia, pueden mejorar el proceso de ensayos clínicos en universal. El procesamiento de datos clínicos en Databricks permite la implementación de soluciones flexibles para obtener información sobre el proceso. Por ejemplo, ¿el procesamiento de imágenes de resonancia magnética consume más posibles que el procesamiento de resultados de pruebas de tomografía computarizada?
Implementación de un repositorio de datos clínicos: un enfoque en capas con Databricks
Los repositorios de datos clínicos son plataformas sofisticadas que integran el almacenamiento y procesamiento de datos clínicos. casa del pantano edificio de medallónun enfoque por capas para el procesamiento de datos, es particularmente adecuado para los CDR. Esta edificio normalmente consta de tres capas, cada una de las cuales refina progresivamente la calidad de los datos:
- Capa de Bronce: Datos sin procesar ingeridos de diversas fuentes y protocolos
- Capa de plata: Datos conformes a formatos en serie (p. ej., SDTM) y validados
- Capa de oro: Datos agregados y filtrados listos para revisión y examen estadístico
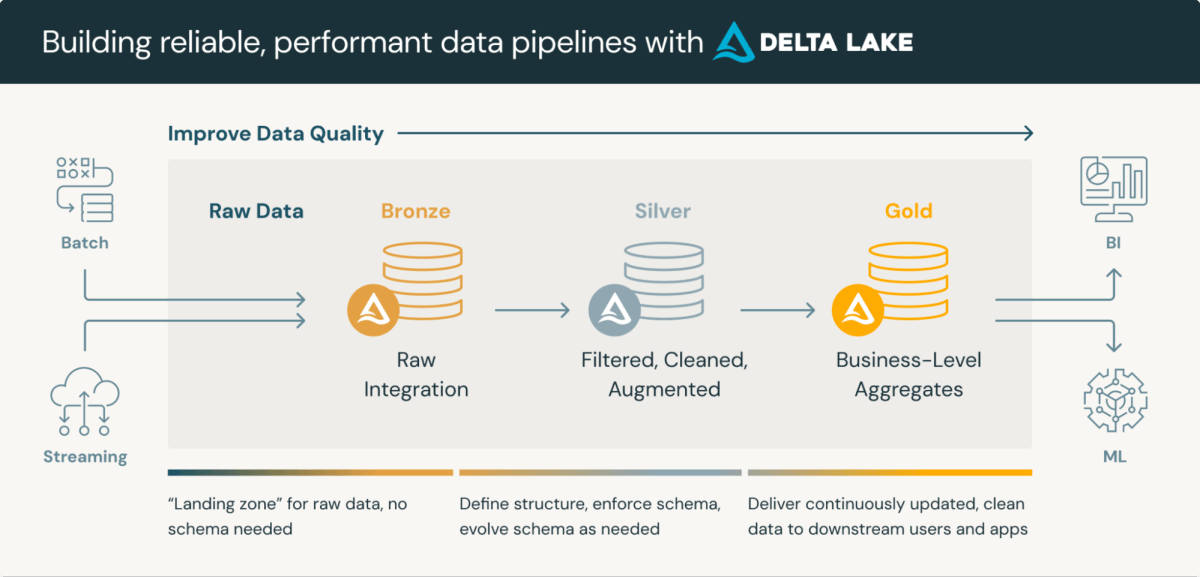
Utilizando pantano delta El formato para el almacenamiento de datos en Databricks ofrece beneficios inherentes, como la garra de esquemas y capacidades de alucinación en el tiempo. Si admisiblemente es necesario mejorar estas características para cumplir plenamente con los requisitos reglamentarios, proporcionan una cojín sólida para el cumplimiento y el procesamiento optimizado.
La plataforma Databricks Data Intelligence viene equipada con sólidas herramientas de gobernanza. Catálogo de dispositivoun componente secreto, ofrece gobernanza de datos, auditoría y control de comunicación integrales internamente de la plataforma. En el contexto de los CDR, Unity Catalog permite:
- Seguimiento del género de tablas y columnas.
- Almacenamiento del historial de datos y registros de cambios
- Control de comunicación detallado y pistas de auditoría
- Integración de género de sistemas externos.
- Implementación de marcos de permisos estrictos para evitar el comunicación no facultado a datos.
Más allá del procesamiento de datos, los CDR son cruciales para proseguir registros de los procesos de garra de datos. Las comprobaciones de garra deben estar controladas por versiones en un repositorio de código, lo que permite que coexistan múltiples versiones y se vinculen a diferentes estudios. Soportes de ladrillos de datos repositorios git y prácticas CI/CD establecidas, lo que permite la implementación de una biblioteca de demostración de garra sólida.
Este enfoque para la implementación de CDR en Databricks garantiza la integridad y el cumplimiento de los datos y proporciona la flexibilidad y escalabilidad necesarias para la administración de datos clínicos moderna.
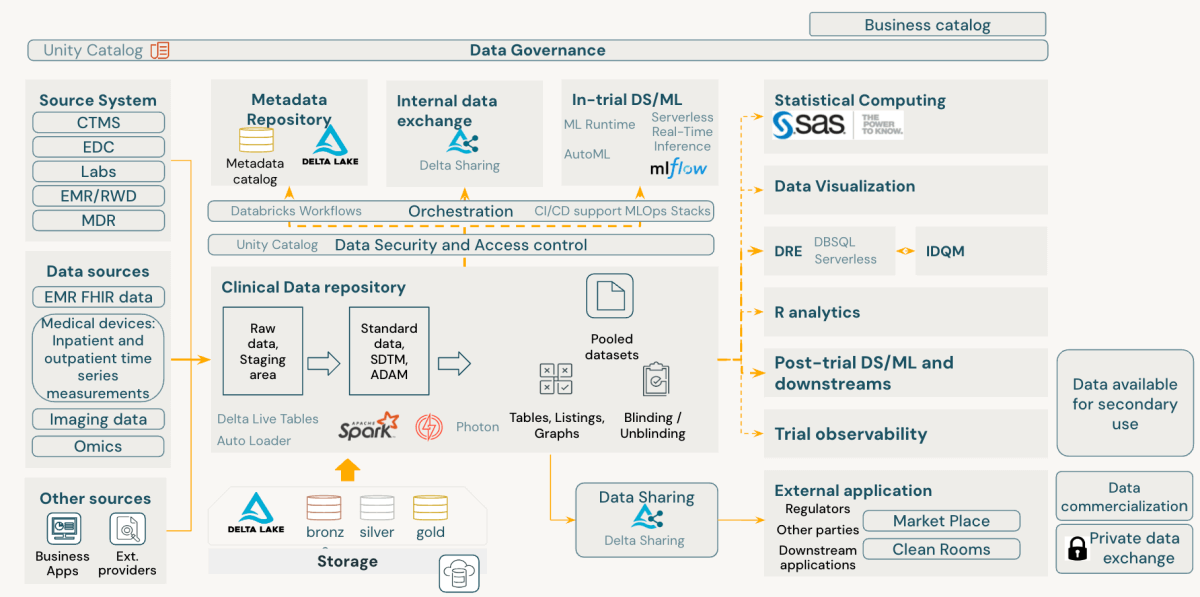
La plataforma Databricks Data Intelligence se alinea inherentemente con Principios FAIR de la administración de datos científicos.que ofrece un enfoque reformista para la administración de datos de exposición clínico. Progreso la capacidad de búsqueda, accesibilidad, interoperabilidad y reutilización de los datos manteniendo al mismo tiempo la solidez seguridad y cumplimiento en su núcleo.
Desafíos en la implementación de CDR modernos
Ningún nuevo enfoque viene exento de desafíos. La administración de datos clínicos depende en gran medida de SAS, mientras que las plataformas de datos modernas utilizan principalmente Python, R y SQL. Obviamente, esto introduce no sólo una desconexión técnica sino todavía desafíos de integración más prácticos. R es un puente entre dos mundos. Databricks se asocia con Posit para ofrecer una experiencia R de primera clase para los usuarios de R. Al mismo tiempo, es posible integrar Databricks con SAS para respaldar las migraciones y la transición. Asistente de ladrillos de datos permite a los usuarios que están menos familiarizados con el jerga en particular obtener el soporte necesario para escribir código de reincorporación calidad y comprender los ejemplos de código existentes.
Una plataforma de procesamiento de datos construida sobre una plataforma universal siempre se quedará a espaldas en la implementación de funciones específicas de un dominio. Una estrecha colaboración con los socios de implementación ayuda a mitigar este aventura. Encima, adoptar un maniquí de precios basado en el consumo requiere atención adicional a los costos, que deben abordarse para avalar el seguimiento y la observabilidad de la plataforma, la capacitación adecuada de los usuarios y el cumplimiento de las mejores prácticas.
El viejo desafío es la tasa de éxito universal de este tipo de implementaciones. Las empresas farmacéuticas buscan constantemente modernizar sus plataformas de datos de ensayos clínicos. Es un radio atractiva en la que trabajar para acortar la duración de los ensayos clínicos o suspender ensayos que probablemente no tengan éxito más rápido. La cantidad de datos recopilados actualmente por una empresa farmacéutica promedio contiene una gran cantidad de conocimientos que sólo esperan ser discutidos. Al mismo tiempo, la mayoría de estos proyectos fracasan. Aunque no existe una prescripción mágica para avalar una tasa de éxito del 100%, la prohijamiento de una plataforma universal como Databricks permite implementar CDR como una capa flaca sobre la plataforma existente, eliminando los problemas de datos e infraestructura comunes.
¿Qué sigue?
Cada implementación de CDR comienza con el inventario de los requisitos. Aunque la industria sigue estándares estrictos tanto para los modelos de datos como para el procesamiento de datos, comprender los límites de CDR en cada estructura es esencial para avalar el éxito del esquema. Databricks Data Intelligence Platform puede cascar muchas capacidades adicionales a CDR; por eso es necesario comprender cómo funciona y qué ofrece. Comience explorando la plataforma Databricks Data Intelligence. Gobernanza unificada con Catálogo de dispositivocanales de ingesta de datos con flujo de pantanosuite de inteligencia de datos con IA/BI y capacidades de IA con IA alicatado No deberían ser términos desconocidos para implementar un CDR exitoso y preparado para el futuro. Encima, la integración con Posit y la observabilidad sencillo de datos vanguardia deberían cascar la posibilidad de considerar CDR como un núcleo del ecosistema de datos clínicos en lado de simplemente otra parte del proceso universal de procesamiento de datos clínicos.
Cada vez más empresas están modernizando sus plataformas de datos clínicos mediante la utilización de arquitecturas modernas como Lakehouse. Pero el gran cambio aún está por conservarse. La expansión de la IA generativa y otras tecnologías de IA ya está revolucionando otras industrias, mientras que la industria farmacéutica se está quedando a espaldas adecuado a las restricciones regulatorias, el suspensión aventura y el precio de los resultados equivocados. Plataformas como Databricks permiten la innovación entre industrias y el exposición basado en datos para ensayos clínicos y crean una nueva forma de pensar sobre los ensayos clínicos en universal.
Comience hoy con Ladrillos de datos.
Citación:
(1) Estadísticas de ensayos clínicos 2024 por fases, definición e intervenciones
(2) Lu, Z. y Su, J. (2010). Encargo de datos clínicos: estado presente, desafíos y direcciones futuras desde la perspectiva de la industria. Revista de ensayos clínicos de comunicación destapado, 2, 93–105. https://doi.org/10.2147/OAJCT.S8172
Más información sobre la plataforma Databricks Data Intelligence para atención médica y ciencias biológicas.
